
- Auteur Stanley Ellington ellington@answers-business.com.
- Public 2023-12-16 00:16.
- Dernière modifié 2025-01-22 15:59.
La diffusion de tout fluide, gaz molécules de faible concentration à haute concentration de solutés qui est facilitée par la présence de la membrane semi-perméable est appelé « Osmose ». Les molécules d'eau se déplacent du bas pression osmotique au plus haut région de pression osmotique.
De plus, l'eau passe-t-elle d'une concentration de soluté faible à élevée ?
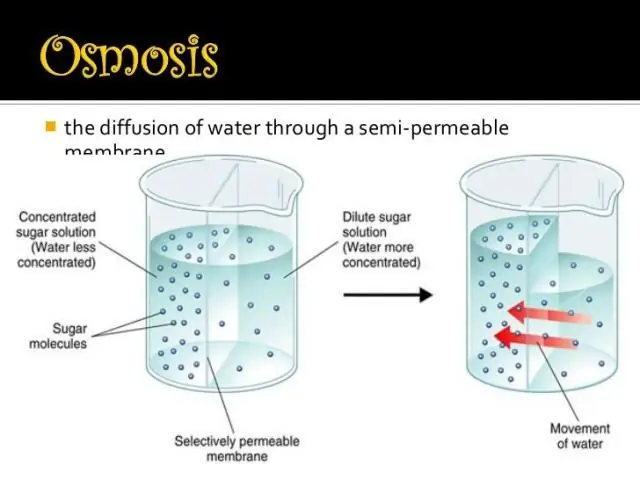
Osmose: En osmose, l'eau toujours se déplace d'une zone de concentration en eau plus élevée à l'un des concentration plus faible . Dans le schéma présenté, le soluté ne peut pas traverser la membrane sélectivement perméable, mais le l'eau pouvez.
Aussi, que signifie une concentration élevée d'eau? Les concentration en eau peut être considérée comme la proportion d'une solution qui est l'eau . Des solutions avec un haute concentration des molécules de soluté, comme les sucres ou les sels, ont une faible concentration d'eau molécules et vice versa.
En conséquence, qu'est-ce qui passe d'une concentration faible à une concentration élevée ?
La diffusion est un mouvement spontané de particules à partir d'une zone de haute concentration à une zone de faible concentration . L'osmose est le mouvement net spontané de l'eau à travers une membrane semi-perméable à partir d'une région de meugler soluté concentration à une solution plus concentrée, jusqu'à un concentration pente.
La concentration hypertonique est-elle faible à élevée?
Hypertonique : La solution avec le concentration plus élevée de solutés. Hypotonique: La solution avec le concentration plus faible de solutés.
Conseillé:
Lorsque vous avez une réactivité nationale élevée et une intégration mondiale élevée, cela s'appelle-t-il ?

Question 5 5 points sur 5 Lorsque vous avez une réactivité nationale élevée et une intégration mondiale élevée, cela s'appelle? Réponse choisie : Stratégie transnationale. Bonne réponse : stratégie transnationale
Qu'est-ce qu'une implication élevée et faible ?

Les produits à forte implication sont ceux qui représentent la personnalité, le statut et le style de vie du consommateur; par exemple, l'achat d'un cinéma maison. En revanche, les produits à faible implication sont ceux qui reflètent des décisions d'achat de routine; par exemple, acheter un bonbon ou une glace
Quand les molécules descendent leur gradient de concentration ?

Gradients de concentration. Un gradient de concentration se produit lorsque la concentration de particules est plus élevée dans une zone que dans une autre. Dans le transport passif, les particules diffuseront le long d'un gradient de concentration, des zones de concentration plus élevée aux zones de concentration plus faible, jusqu'à ce qu'elles soient uniformément espacées
Que se passe-t-il lorsque la concentration de glucose dans l'eau à l'extérieur d'une cellule est supérieure à la concentration à l'intérieur ?
Si la concentration de glucose dans l'eau à l'extérieur d'une cellule est supérieure à la concentration à l'intérieur, l'eau aura tendance à quitter la cellule par osmose. c. le glucose aura tendance à entrer dans la cellule par osmose
La demande pour le prix des iPhones est-elle inélastique ou élastique Pourquoi l'élasticité-revenu est-elle élevée ou faible ?

Par conséquent, on peut dire que l'iPhone est élastique au revenu, car il a une valeur supérieure à 1. C'est un bien normal car le pourcentage d'augmentation de la quantité demandée est supérieur au pourcentage d'augmentation du revenu. Une augmentation des revenus conduirait certainement à une augmentation de la demande pour de tels biens
